北京2026年1月6日 /美通社/ -- 近日,一项由中国疾病预防控制中心牵头的全国多中心研究证实:万泰生物尿液HIV-1胶体金法自测试剂盒在真实世界中表现出99.44%灵敏度与100%特异性的卓越诊断性能。同时,其简单易用、隐私性高的操作流程受到用户的广泛好评,该研究发表于Nature子刊Scientific Reports。

核心研究亮点
证据扎实、表现优秀的诊断性能
该研究由中国疾病预防控制中心艾防中心牵头,在北京、河南、云南三省开展,纳入1495名参与者,研究中使用万泰生物尿液HIV-1胶体金法自测试剂盒与金标准Western blot检测进行结果比对,结果显示:在未接受抗病毒治疗人群中,尿液HIV自测试剂的灵敏度达99.44%,特异性达100%,PPV为100%,NPV为99.81%,与金标准的符合率达99.86%,该诊断性能与基于血液样本的ELISA检测结果高度一致。
表1 尿液HIV-1自测试剂盒与金标准的检测结果比对
Western Blot检测(金标准)
合计
阳性
阴性
HIV-1自检试剂盒检测
阳性
357
357
阴性
2
1044
1046
合计
359
1044
1403
无监督场景具备高可靠性
患者在家庭自测的结果与在机构开展检测的结果高度一致,证实尿液HIV自测试剂在去中心、无监督场景下的检测结果可靠性,解决了传统自测产品因操作环境差异导致的准确性疑虑。
表2 家庭环境与机构环境的检测结果比对
开展地点
家庭环境
医疗机构
阳性例数
5
5
阴性例数
102
102
Kappa一致性系数
1.000
用户体验获高度认可
问卷调查结果显示,98.21%的受访者可独立完成操作,93.04%的受访者在样本收集、结果判读等关键步骤操作准确规范。
针对尿液HIV-1自测产品,用户满意度达97.84%,尤其受女性、年轻群体(18–50岁)及高教育水平者认可。
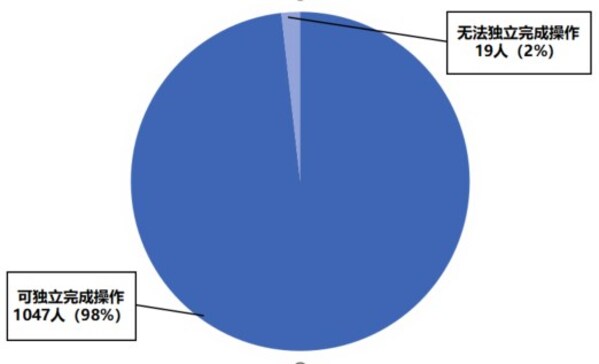
用户体验调查结果
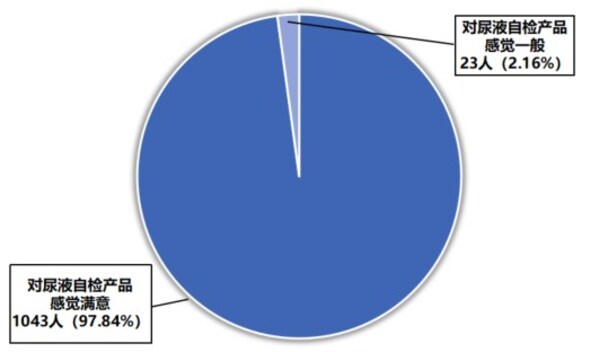
用户体验调查结果
本研究由中国疾病预防控制中心艾防中心主导,覆盖多地域、多人群,是迄今中国最大规模的尿液HIV自测试剂真实世界评估。其扎实的研究证据,不仅验证了产品的临床可靠性,更确立了其在HIV自测市场的技术标杆地位。结合高用户接受度及与家庭自测场景的完美适配性,本产品有望成为推动中国实现"95-95-95"目标的关键工具。
破解HIV检测"最后一公里"难题
在我国,HIV感染人群的知晓率仅为84%,是我国实现"95-95-95"全球防控目标的最大的挑战,快速、便捷的艾滋病自我检测试剂是促进人群检测意愿,提高HIV感染人群知晓率及检测率的良好助力。
尿液HIV自测产品与本研究的研究结果直指中国现阶段的HIV防控核心痛点,尿液自测凭借隐私性、无创性和可及性,能有效覆盖高风险但拒检人群(如MSM群体、高校人群)。
HIV全样本一体化自测解决方案
WHO于2024年公布了《差异化HIV检测服务的综合指南》,强调了基于多元化检测方法及自我检测策略在HIV防控工作中的重要性。为了响应不同人群的自我检测需求,近日,万泰生物推出了国内首个"血-尿-唾"一体化自测解决方案"。
万泰生物此次推出的HIV全样本一体化自测解决方案,首次实现了三类样本自测产品的系统化整合:
血液检测(国械注准20173401137):延续经典检测路径,适用于注重高精准度结果、具备采血条件的人群,其灵敏度与特异性均达99%以上;
尿液检测(国械注准 20193400550&国械注准20253402651):HIV-1尿液自测试剂已于2025年通过世界卫生组织PQ认证,成为HIV尿液自测的首创试剂,升级后HIV1+2尿液自测试剂也于2025年底同步获批。取样直观且无采样手法带来的差异,适用于隐私要求高、恐针或静脉条件受限者;
唾液检测(国械注准20253402650):首家唾液无创自测方案,解决了"当面共检"时的隐私与尴尬,同时适用于儿童、应急筛查及极端隐私敏感人群。
响应国策,助力防艾落地
《中国遏制与防治艾滋病规划(2024—2030年)》明确提出"创新检测服务模式,最大限度发现感染者"。万泰生物以科技创新支撑公共卫生目标,HIV全样本一体化自测解决方案恰好为国内防艾政策最好落地工具——让检测从专业机构走向家庭,从被动等待走向主动筛查。






 加载中,请稍侯......
加载中,请稍侯......